3 xeitos emocionantes nos que os químicos construíron compostos este ano
por Bethany Halford
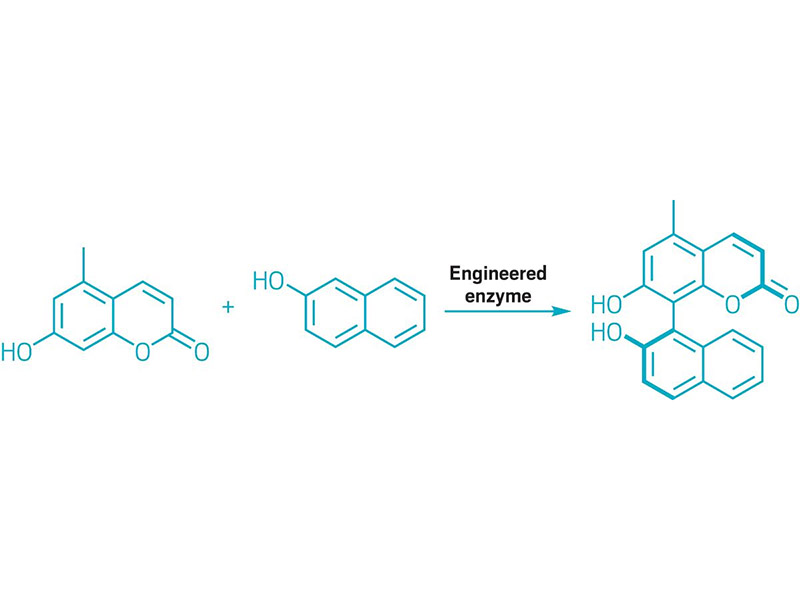
AS ENCIMAS EVOLUCIONADAS CONSTRUÍRON ENLACES DE BIARILO
Esquema que mostra un acoplamento de biarilo catalizado por encimas.
Os químicos empregan moléculas de biarilo, que presentan grupos arilo unidos entre si por un enlace simple, como ligandos quirais, materiais como bloques de construción e produtos farmacéuticos. Pero a creación do motivo de biarilo con reaccións catalizadas por metais, como os acoplamentos cruzados de Suzuki e Negishi, normalmente require varios pasos sintéticos para crear os socios de acoplamento. Ademais, estas reaccións catalizadas por metais fallan ao fabricar biarilos voluminosos. Inspirado pola capacidade dos encimas para catalizar reaccións, un equipo dirixido por Alison RH Narayan, da Universidade de Michigan, utilizou a evolución dirixida para crear un encima de citocromo P450 que constrúe unha molécula de biarilo mediante o acoplamento oxidativo de enlaces carbono-hidróxeno aromáticos. O encima une moléculas aromáticas para crear un estereoisómero arredor dun enlace con rotación impedida (mostrado). Os investigadores cren que esta estratexia biocatalítica podería converterse nunha transformación básica para crear enlaces biarilo (Nature 2022, DOI: 10.1038/s41586-021-04365-7).

RECEITA PARA AMINAS TERCIARIAS BASEADA NUN POUCO SAL
O esquema mostra unha reacción que produce aminas terciarias a partir de aminas secundarias.
A mestura de catalizadores metálicos sedentos de electróns con aminas ricas en electróns normalmente mata os catalizadores, polo que os reactivos metálicos non se poden usar para construír aminas terciarias a partir de aminas secundarias. M. Christina White e os seus colegas da Universidade de Illinois Urbana-Champaign déronse conta de que podían solucionar este problema se engadían algún condimento salgado á súa receita de reactivos. Ao transformar as aminas secundarias en sales de amonio, os químicos descubriron que podían reaccionar estes compostos con olefinas terminais, un oxidante e un catalizador de sulfóxido de paladio para crear unha infinidade de aminas terciarias cunha variedade de grupos funcionais (móstrase un exemplo). Os químicos usaron a reacción para fabricar os fármacos antipsicóticos Abilify e Semap e para transformar fármacos existentes que son aminas secundarias, como o antidepresivo Prozac, en aminas terciarias, demostrando como os químicos poderían crear novos fármacos a partir dos xa existentes (Science 2022, DOI: 10.1126/science.abn8382).
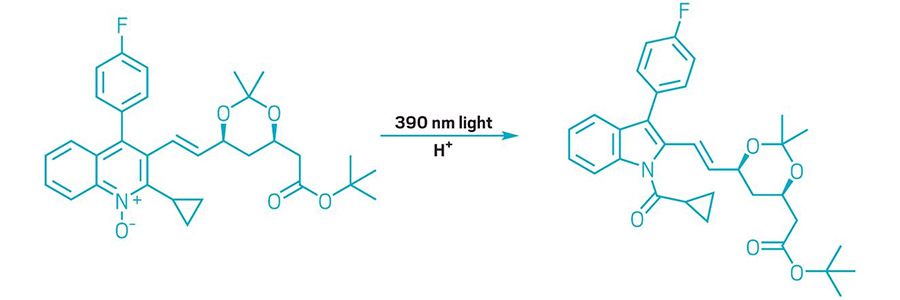
OS AZAARENOS SUFRIU UNHA CONTRACCIÓN DE CARBONO
O esquema mostra un N-óxido de quinoleína transformado nun N-acilindol.
Este ano, os químicos ampliaron o repertorio da edición molecular, que son reaccións que producen cambios nos núcleos de moléculas complexas. Nun exemplo, os investigadores desenvolveron unha transformación que usa luz e ácido para recortar un só carbono de azaarenos de seis membros en N-óxidos de quinoleína para formar N-acilindoles con aneis de cinco membros (móstrase un exemplo). A reacción, desenvolvida por químicos do grupo de Mark D. Levin na Universidade de Chicago, baséase nunha reacción que implicaba unha lámpada de mercurio, que emitía múltiples lonxitudes de onda de luz. Levin e os seus colegas descubriron que o uso dun díodo emisor de luz que emite luz a 390 nm lles proporcionaba un mellor control e permitíalles facer a reacción xeral para os N-óxidos de quinoleína. A nova reacción ofrece aos fabricantes de moléculas unha forma de remodelar os núcleos de compostos complexos e podería axudar aos químicos medicinais que buscan ampliar as súas bibliotecas de candidatos a fármacos (Science 2022, DOI: 10.1126/science.abo4282).
Data de publicación: 19 de decembro de 2022

